La diferencia entre combustible y comburente radica en sus roles en una reacción de combustión. El combustible es la sustancia que se quema, liberando energía, mientras que el comburente es el agente que proporciona el oxígeno necesario para que dicha combustión ocurra eficientemente.
La diferencia entre combustible y comburente es un tema esencial para comprender cómo se producen las reacciones químicas que liberan energía, especialmente en procesos como la combustión. En este artículo, se explorarán las características distintivas de ambos términos, con la finalidad de proporcionar una comprensión clara y detallada que permita a los usuarios diferenciar entre uno y otro fácilmente.
Tabla de contenidos
ToggleDefinición de combustible
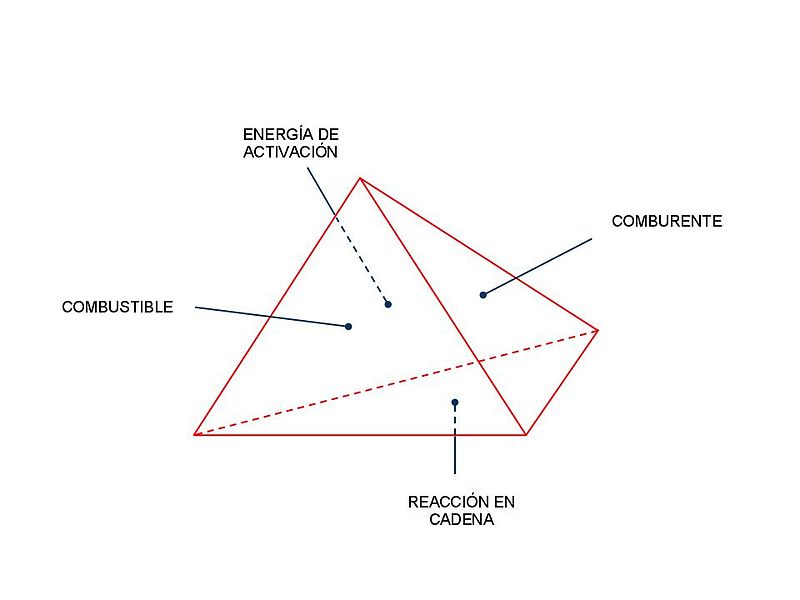
El combustible es una sustancia que, al reaccionar con un comburente, libera energía en forma de calor y luz. Los combustibles pueden ser sólidos, líquidos o gaseosos y son esenciales en numerosos procesos industriales, domésticos y de transporte. Ejemplos comunes incluyen la madera, el carbón, el petróleo y el gas natural.
Tipos de combustibles
Los combustibles pueden clasificarse en varias categorías según su estado físico y origen:
- Combustibles fósiles: Incluyen carbón, petróleo y gas natural. Son derivados de la descomposición de materia orgánica antigua.
- Combustibles renovables: Como la biomasa y los biocombustibles, son obtenidos de fuentes que se regeneran rápidamente.
- Combustibles sólidos: Ejemplos son la madera y el carbón.
- Combustibles líquidos: Tales como el petróleo y sus derivados.
- Combustibles gaseosos: Como el metano y el propano.
Definición de comburente
El comburente es la sustancia que permite la combustión de un combustible. Es, típicamente, un gas que suministra oxígeno, el cual es un elemento esencial para que se produzca la reacción de combustión. El oxígeno en el aire es el comburente más común, aunque otros gases como el flúor y el cloro también pueden actuar como comburentes.
Propiedades del comburente
Los comburentes poseen ciertas propiedades específicas que los hacen adecuados para facilitar la combustión:
- Alta reactividad química: Capacidad para reaccionar con el combustible.
- Disponibilidad: El oxígeno es abundante en la atmósfera, lo que facilita su uso.
- Capacidad oxidante: Capacidad para aceptar electrones y formar nuevos compuestos.
Proceso de combustión
La combustión es una reacción química entre un combustible y un comburente, típicamente oxígeno, que libera energía en forma de calor y luz. Este proceso es fundamental en diversas aplicaciones, desde la generación de energía hasta la propulsión de vehículos.
Fases de la combustión
El proceso de combustión puede dividirse en varias fases:
- Premezcla: El combustible y el comburente se mezclan antes de la ignición.
- Ignición: Se inicia la reacción química mediante una fuente de calor.
- Propagación: La reacción se propaga liberando calor y luz.
- Extinción: La combustión se detiene cuando uno de los reactivos se agota.
Principales diferencias entre combustible y comburente
Las principales diferencias entre combustible y comburente pueden resumirse de la siguiente manera:
- Naturaleza: El combustible es la sustancia que se quema, mientras que el comburente es la sustancia que facilita la quema.
- Función: El combustible libera energía al reaccionar, el comburente permite esta reacción al proporcionar oxígeno u otro agente oxidante.
- Ejemplos: Ejemplos de combustibles incluyen madera, carbón y gas natural. Ejemplos de comburentes incluyen oxígeno, cloro y flúor.
- Estado físico: Los combustibles pueden ser sólidos, líquidos o gaseosos, mientras que los comburentes suelen ser gases.
Ambos desempeñan roles fundamentales en la combustión y la generación de energía, y su correcto manejo y utilización son esenciales para la eficiencia y la seguridad en estos procesos.